Белки играют центральную роль в существовании всего живого на земле. Кожа и волосы, мышцы и ферменты, гормоны и рецепторы гормонов, пчелиный яд и паутина — все это белки.
С точки зрения химии белки — последовательность аминокислот, соединенных пептидной связью (отсюда их другое название — полипептиды); все многообразие белков построено всего из 20 аминокислот.
Одной из важных причин, вызывающих интерес к коротким пептидным последовательностям, стала их способность самоорганизовываться в устойчивые супрамолекулярные структуры. В медицине примером таких структур могут служить амилоидные волокна — они образуются при болезни Альцгеймера или прионных заболеваниях (коровье бешенство) из-за ненормальной организации аминокислот. Механизм возникновения этих заболеваний до сих пор не ясен, но страдания вызываются неконтролируемой сборкой пептидов в необычайно устойчивые волокна со структурой бета-слоев, т.н. бета-амилоиды. Эти волокна практически не поддаются протеолизу и не разрушаются даже при стерилизации в автоклаве (120 ?С).
В 1993 году в журнале "Записки национальной академии наук США" вышла работа Чжана Сюгуана из Массачусетского технологического института — с описанием спонтанного формирования мембраны из раствора короткого пептида ЕАК16 (последовательность [AEAEAKAK]2) при увеличении концентрации солей моновалентных ионов (Li+, Na+, K+, или Cs+). Электронно-микроскопические изображения показали, что на самом деле мембрана состоит из отдельных волокон диаметром 10-20 нанометров. Так же как и амилоидные волокна, волокна ЕАК16 обладали структурой бета-слоя, были устойчивы к протеолизу и не меняли своей структуры при нагреве по крайней мере до 90 градусов даже в присутствии додецилсульфата натрия или мочевины — веществ, обычно использующихся для денатурации белков.
Как позже писал сам Чжан, открытие он сделал случайно, изучая геном обычных пекарских дрожжей, но оно дало толчок к развитию целого направления: стало ясно, что можно создавать самоорганизующиеся биологические материалы под заказ. Вскоре Чжан c коллегами создали новый пептид, обладающий аналогичными свойствами — RADA16 (последовательность RADARADARADARADA).
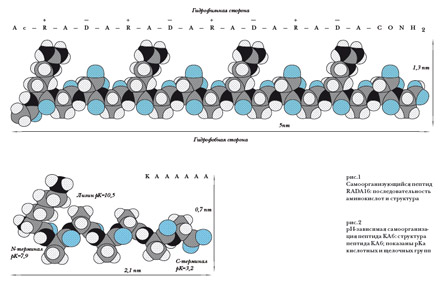
В чем же секрет пептидов EAK16 и RADA16? Как видно на рисунке 1, на примере пептида RADA16, одна сторона молекулы содержит только гидрофобные группы, а другая — гидрофильные группы с чередованием положительных и отрицательных зарядов. В водном растворе молекулы могут уменьшить свою энергию, став "спиной к спине" и скрыв гидрофобную сторону от молекул воды. Следующая пара молекул может подойти к первой и расположиться так, чтобы ее положительные заряды совпали с отрицательными зарядами первой — и наоборот. Так образуется длинное пептидное волокно, которое точнее следовало бы назвать пептидной лентой. Волокна в процессе роста переплетаются друг с другом и образуют гидрофильную матрицу, гидрогель, содержащий 99,5-99,9% воды.
Такие гидрофильные матрицы, построенные из пептидов, оказались крайне интересны для такой быстроразвивающейся области бионанотехнологий, как создание тканей организма из стволовых клеток. Эксперименты, проведенные в разных лабораториях, показали успешный рост и дифференциацию в пептидных матрицах культур нейронных стволовых клеток и миоцитов сердца. В одном из экспериментов перерезанный оптический нерв хомяка восстановился после введения пептидной матрицы в область разреза: нейроны мигрировали в матрицу и образовали новые соединения взамен поврежденных. Есть надежда, что в скором будущем такие пептидные матрицы помогут людям излечивать последствия мозговых травм, инсульта, бороться с возрастными изменениями в мозге. Это серьезный прорыв, приближающий науку к более полному использованию регенеративных возможностей стволовых клеток.
Конструируя последовательность короткого пептида, мы можем управлять электростатическими, гидрофобными и ван-дер-ваальсовыми взаимодействиями и, таким образом, создавать самоорганизующуюся супрамолекулярную структуру желаемой геометрии. Вероятно, наиболее исследованный тип самоорганизации наблюдается в поверхностно-активных веществах (ПАВ). При концентрации выше критической эти молекулы начинают собираться в мицеллы, причем структура мицелл определяется геометрией молекулы: в зависимости от соотношения размеров гидрофильной и гидрофобной частей молекулы, мицеллы могут быть сферическими или цилиндрическими или образовывать плоские слои наподобие лазаньи. Типичная молекула ПАВ состоит из гидрофобного "хвоста" и гидрофильной "головы". Как было показано в работах Чжана, пептид, созданный по такому рецепту, например V6D (последовательность VVVVVVD), будет вести себя как поверхностно-активное вещество и при концентрации выше критической образовывать цилиндрические мицеллы и растворять гидрофобные вещества, захватывая их во внутреннюю часть мицеллы.
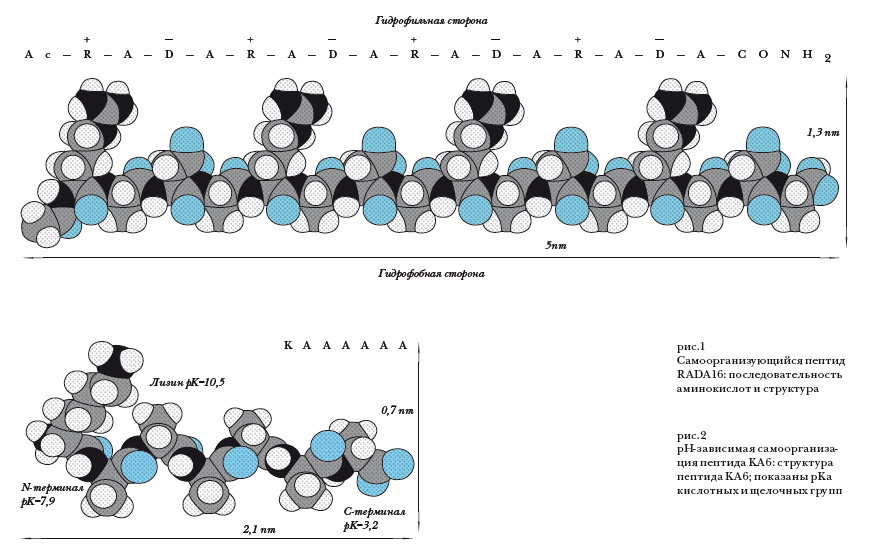
Работа, опубликованная группой Петера Фойана и автора этих строк из Университета Ольборга в Journal of Nanoscience and Nanotechnology, открывает другую возможность использования поверхностно-активных пептидов. Авторы синтезировали пептиды из семи аминокислот, в которых центральная часть пептидной цепочки гидрофобна, а концы несут электрический заряд, появляющийся или исчезающий в зависимости от кислотности раствора. При pH<3, кислотный С-терминал протонируется и теряет отрицательный заряд, в то время как щелочной N-терминал и лизин несут положительный заряд, в нейтральной среде оба конца несут заряды, положительный и отрицательный, а в щелочной среде N-терминал и лизин теряют свой заряд, и молекула становится отрицательно заряженной. Таким образом, можно не только поменять эффективный размер гидрофильной "головы" поверхностно активного пептида, но и поменять "голову" и "хвост" местами. Измерения зета-потенциала на поверхности частиц показали, что, действительно, пептидные мицеллы в кислотной или нейтральной среде несут на поверхности положительный заряд, а в щелочном растворе выворачиваются наизнанку и становятся отрицательно заряженными. Больший размер и больший суммарный положительный заряд N-терминала и лизина сдвигает этот переход в область высоких pH. Из-за несимметричной формы использованных пептидных молекул форма мицелл также отличается в кислотной и щелочной среде. В кислотном и нейтральном растворе пептиды собираются в трубки, а в щелочном — образуют сферы (Рисунок 2). Независимо от заряда на поверхности пептидные мицеллы, так же как и мицеллы обычных поверхностно активных веществ, могут нести в своей сердцевине гидрофобные молекулы.
Если мы, например, загрузим гидрофобное лекарство в такую мицеллу в кислотной среде, то лекарство, не пострадав, пройдет через желудок пациента и будет выгружено из мицеллы в щелочной среде кишечника. А мицеллы, созданные и загруженные в щелочной среде, могут быть использованы для доставки лекарств в опухоли или очаги воспаления, которые обычно характеризуются кислотной средой. Подобные системы доставки лекарств уже активно разрабатываются — но с использованием синтетических полимеров. У полипептидов — существенное преимущество перед синтетикой: они легко выводятся из организма и не накапливаются во внутренних органах.
Литература
S. Zhang et al., "Spontaneous assembly of a self-complementary oligopeptide to form a stable macroscopic membrane", PNAS 90, 3334-3338 (1993)
С.Hauser and S.Zhang, "Designer self-assembling peptide nanofiber biological materials", Chem.Soc.Rev. 39, 2780-2790 (2010)
L. Gurevich et al, "pH-dependent self-assembly of short surfactant-like peptide KA6", J.Nanosci.Nanotechnol. 10, 7946-7950 (2010)

