В России — четвертая, самая высокая волна коронавируса, медицина работает с огромной перегрузкой. Как нельзя более вовремя состоялась регистрация первого отечественного внутривенного противовирусного препарата прямого действия «Арепливир» (международное непатентованное название — фавипиравир). До конца года лекарство поступит в стационары всех регионов. Академик РАН Дмитрий Пушкарь подчеркивает: «Во всем мире есть две компании, производящие инъекционный препарат прямого противовирусного действия от ковида. И одна — российская!»
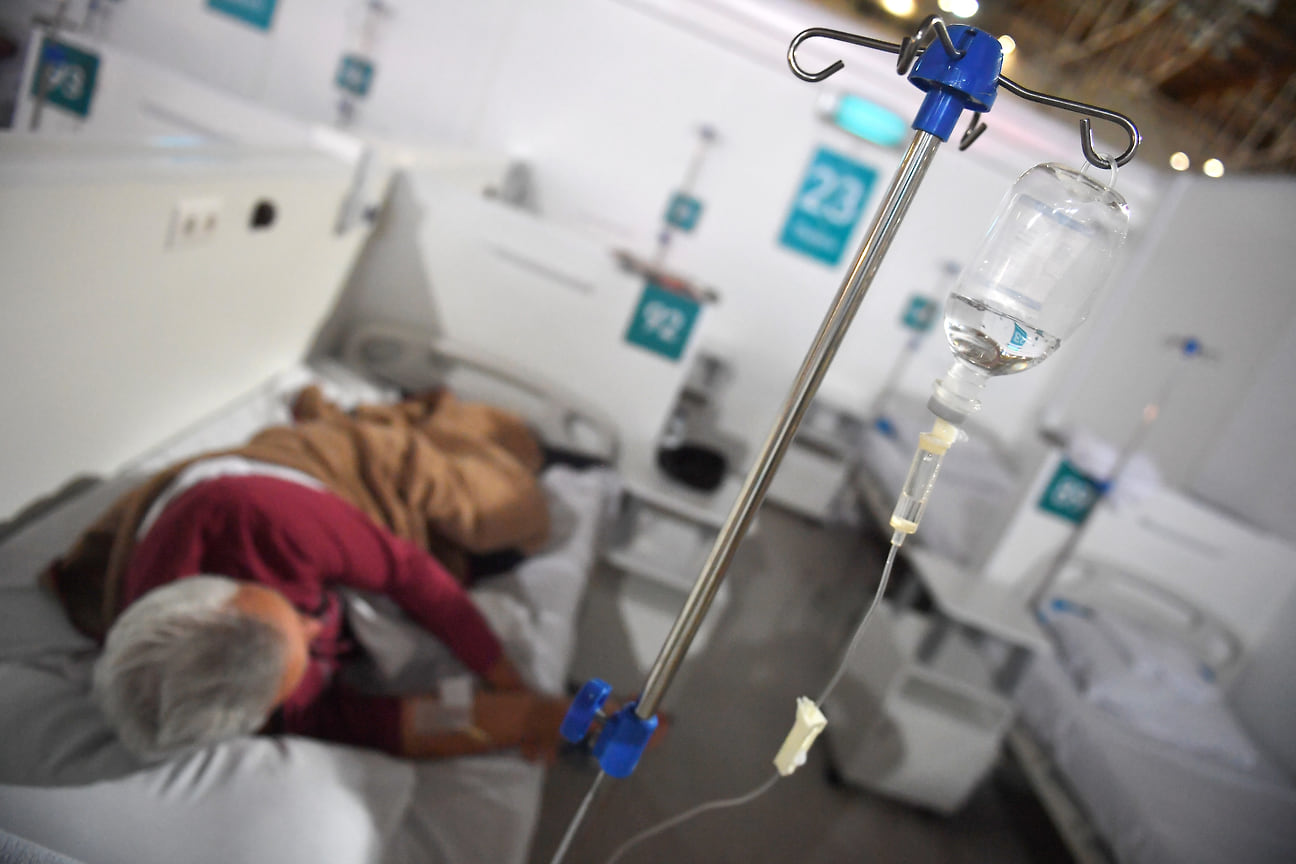
Фото: Александр Миридонов, Коммерсантъ
Фото: Александр Миридонов, Коммерсантъ
Как следует из государственного реестра лекарственных средств, первый в России препарат от ковида в форме инъекций «Арепливир» зарегистрирован 12 ноября, ему разрешен ввод в гражданский оборот на пять лет.
«Сейчас разрабатываются и в принципе в ближайшее время будут уже, уверен, использоваться лекарственные препараты [против ковида]»,— сообщил на совещании с руководством Министерства обороны России и предприятий оборонно-промышленного комплекса России президент Владимир Путин. Одним из первых таких препаратов и стал инъекционный «Арепливир».
«До сих пор единственным противовирусным препаратом для парентерального введения было иностранное средство, не только дорогостоящее, но и малодоступное,— разъясняет ситуацию главный пульмонолог Минздрава, член-корреспондент РАН Сергей Авдеев.— "Промомед" предложил новый класс лекарств, который способен кардинально изменить ситуацию с госпитализированными больными — наиболее рискованной когортой пациентов». Академик Авдеев уверен, что появление эффективного и широко доступного отечественного противовирусного лекарственного средства для парентерального введения способно переломить ход борьбы с пандемией. «Инъекционную форму препарата характеризует не только стопроцентная биодоступность, но и более интенсивное проникновение и распределение в клетках, более длительное удержание терапевтической концентрации в тканях, а также улучшенный профиль безопасности. Это должно значительно повысить эффективность проводимого лечения на госпитальном этапе»,— заключает Сергей Авдеев.
«Клиническое исследование показало преимущество применения "Арепливира" по сравнению со стандартной терапией в отношении улучшения клинического статуса,— информирует Кира Заславская, директор по новым продуктам ГК "Промомед".— В частности, по данным исследования, количество пациентов, соответствующих критериям выписки из стационара (статус 0-3 по категориальной шкале ВОЗ), в группе "Арепливира" было в несколько раз больше, чем в группе стандартной терапии. Улучшение состояния сопровождалось нормализацией температуры тела, уровня маркеров воспаления и сатурации, что говорит об положительном влиянии терапии на прогноз в целом».
«Клиницисты видели, что "Арепливир" в таблетках хорошо себя зарекомендовал в терапии ковида, поэтому поставили перед нами задачу создать его в парентеральной форме для лечения на госпитальном этапе,— комментирует Петр Белый, председатель совета директоров ГК "Промомед".— Мы отнеслись к этому очень серьезно и обратились к помощи российских ученых, которые эту задачу выполнили, а мы ее реализовали на производстве. Я считаю критически важным для отечественного здравоохранения иметь собственные разработки и производство инновационных национальных лекарственных средств. Мы рады выполнить свою часть работы в этом направлении и представить препарат, который с нетерпением ждут врачи красных зон».
«Уже с начала декабря компания приступает к промышленному выпуску и сможет обеспечивать организации здравоохранения — госпитали и больницы»,— продолжает Петр Белый.

«Промомед» первым в мире смог сделать инъекционную форму фавипиравира, хотя субстанция представляет собой нерастворимый порошок. Многоцентровое клиническое исследование под руководством академика РАН Дмитрия Пушкаря подтвердило эффективность и безопасность нового препарата при его применении в стационарах: «Исследования инъекционного "Арепливира" были проведены в соответствии со всеми принципами GCP и доказательной медицины, что позволяет не сомневаться в достоверности их результатов. Особенно важно, что на фоне тяжелой коронавирусной инфекции происходит поражение слизистой ЖКТ, что может снизить эффективность пероральных препаратов. Внутривенное введение устраняет эту проблему. На практике была доказана важность наличия внутривенной формы препарата, которая в ряде случаев обеспечивает скорейшее выздоровление, обладая более благоприятным профилем безопасности»,— прокомментировал Дмитрий Пушкарь.
«По мере того как будут проходить регистрационные процедуры и процедуры одобрения препарата в других странах мира, мы, конечно, будем стараться оказывать помощь больным во всем мире,— заявил Петр Белый.— Мы уже знаем, как это работает с таблетками — естественным образом сначала обеспечивается внутренний рынок, потом экстерриториальные. По тому интересу, который мы видели к "Арепливиру" в таблеточной форме, порядка 50 стран заинтересованы в препарате».
«Результаты клинических исследований обязательно будут опубликованы в полном объеме, так же как мы делали по таблеткам, но публикации в уважаемых изданиях требуют времени, в том числе на работу рецензентов. Я хочу обратить внимание, что наши исследования по таблеткам пока являются единственными международно признанными, они прошли рецензирование и опубликованы на ClinicalTrials.gov — это авторитетный международный ресурс по рецензированным клиническим исследованиям — и доступны в самых авторитетных научных источниках. Ровно этим же путем мы идем с клиническими исследованиями внутривенной формы. В команде исследований два академика Российской академии наук, руководит исследованиями академик Дмитрий Пушкарь, удостоенный ордена Пирогова за вклад в борьбу с COVID-19. Исследования выполняются в строгом соответствии с правилами GCP (надлежащая клиническая практика.— «Ъ-Наука»)»,— констатировал Петр Белый. Эти исследования на порядок более сложные, чем исследования в таблеточной форме, но и результаты их еще более интересны клиницистам, объяснил глава ГК «Промомед»: «В скором времени будет опубликован полный отчет в России и на международном уровне, мы, безусловно, сделаем его результаты достоянием общественности».
Пероральная форма «Арепливир» включена в действующие рекомендации как на амбулаторном, так и на стационарном этапах. Ожидается, что и инъекционная форма войдет в рекомендации как более эффективная для лечения госпитализированных пациентов, которым необходим максимально быстрый и клинический подтвержденный результат. Окончательное решение будет принимать Минздрав при очередном пересмотре временных методических рекомендаций «Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19)».
После создания препарата от ковида «Арепливир» в таблетках и ампулах компания-производитель «Промомед» задумывается о разработке способа доставлять лекарство и в наиболее удобной ингаляционной форме.
«Не будем забывать: феномен этой коронавирусной инфекции состоит в том, что вирус впервые за всю историю коронавирусов поселяется не в верхних дыхательных путях, а именно в легких. И в этом смысле местная доставка лекарственных объектов, не только противовирусных, но и коктейля препаратов, видится очень перспективным направлением для лечения коронавируса и для профилактики тяжелых легочных последствий»,— заключает Петр Белый.

