Биохимикам МГУ удалось экспериментально проверить математическую модель того, как один из самых эффективных на данный момент антибиотиков — моксифлоксацин — взаимодействует с клеточной мембраной. Модель подтвердилась. Оказалось, что антибиотик даже слишком хороший.
Фото: Анатолий Жданов, Коммерсантъ / купить фото
Фото: Анатолий Жданов, Коммерсантъ / купить фото
Механизмы устойчивости
Антибиотики воздействуют на различные компоненты клетки возбудителя. В этом отличие антибиотиков от других медикаментов: они устраняют причину заболевания, а не борются с симптомами болезни.
Но патогены совершенствуются, что требует других лекарств, поэтому поиск источников новых антибиотиков — одна из интереснейших задач современных ученых. Существует и другой подход к созданию соединений, обладающих бактерицидным эффектом,— синтетический, однако пока что он не очень эффективен. Особенно учитывая то, что препарат, убивающий микроорганизмы, часто вызывает у пациента неспецифическую реакцию, что связано с воздействием антибиотика на собственные клетки тела. Например, нобелевский лауреат Пауль Эрлих синтезировал и протестировал 606 препаратов, прежде чем найти лекарство от сифилиса, которое лишь незначительно вредило лабораторным мышам и полностью избавляло их от бактерии-возбудителя. Конечно, Эрлих проводил свои исследования в начале XX века и потому не обладал техникой и вычислительными мощностями, которые доступны науке сейчас. Однако и спустя сто лет предсказательной способности алгоритмов все еще недостаточно для того, чтобы быстро смоделировать вещество с необходимой активностью.
Битва бактерий с антибиотиком
Использование антибиотиков сопряжено со сложностями.
Во-первых, постепенно патогенные микроорганизмы могут обрести резистентность к используемым против них средствам. Например, биохимиков, которые долгое время работали со штаммами клеток, устойчивых к канамицину, нельзя им лечить от инфекций, потому что штаммы могли попасть в организм ученых и в результате горизонтального переноса генов привить внешнему патогену устойчивость к данной молекуле. Положительная селекция с геном устойчивости к определенному антибиотику применятся в молекулярной биологии: при выращивании клеточной культуры на чашке Петри в агар — питательную твердую среду для бактерий — добавляется определенный бактерицидный препарат, и выживают только те колонии, которые могут противостоять его действию, получив резистентность в результате деления. Тот же процесс протекает и в нашем организме при несистематическом лечении антибиотиками.
Поколения антибиотиков
Во-вторых, некоторые антибиотики действуют на всю микрофлору, которая есть в организме человека. Известный модельный организм для биологических исследований, кишечная палочка, которая существует в кишечнике теплокровных, тоже может подвергаться атаке антибиотиков наряду с патогенными бактериями. Именно поэтому после курса антибиотиков врачи рекомендуют пить восстанавливающие баланс в пищеварительной системе лекарства и принимать витамин К.
В-третьих, прием антибиотиков связан с побочными эффектами: от головокружения и изменения восприятия вкусов до лейкопении и повреждения суставов. Каким бы ни задумывался эффект фармацевтического препарата, его активное вещество — очень сложная органическая молекула, состоящая из многих атомов, связанных разными взаимодействиями. Она может неспецифично связываться с составляющими эукариотических клеток, повреждая или деформируя их.
Чтобы выяснить, как именно та или иная компонента лекарства воздействует на организм человека, исследователи все чаще используют компьютерное моделирование. С помощью математических расчетов химических, электростатических и других взаимодействий можно предсказать поведение клеток, вблизи которых оказалась молекула антибиотика. Особенно интересно исследовать взаимодействие препаратов с клеточной оболочкой, потому что прежде чем достичь цели, молекулы лекарственного препараты должны миновать множество тканей организма пациента, не нарушив их целостности. Но компьютерное моделирование, каким бы сложным оно ни было, требуют экспериментального подтверждения. И здесь в игру вступают химики-энзимологи.
Антибиотик против оболочки клетки
Сотрудники кафедры химической энзимологии химического факультета МГУ им. М. В. Ломоносова вместе с исследователями ИНЭОС РАН под руководством доктора химических наук Елены Кудряшевой впервые экспериментально проверили математически рассчитанную модель взаимодействия моксифлоксацина с липидной оболочкой клетки. Моксифлоксацин — один из самых действенных антибиотиков широкого спектра, поражающий множество как грамположительных, так и грамотрицательных бактерий-возбудителей. Это противомикробное средство класса фторхинолонов IV поколения, которое с 2012 года включено в Перечень жизненно необходимых и важнейших лекарственных препаратов.
Где в природе искать антибиотики
Структура моксифлоксацина предупреждает его эффлюкс из клетки патогена (из-за дополнительного кольца в положении 7). Он применяется при лечении острого бронхита, внебольничной пневмонии, острого бактериального синусита и прочих заболеваний дыхательных путей, кожных инфекций и поражений мягких тканей.
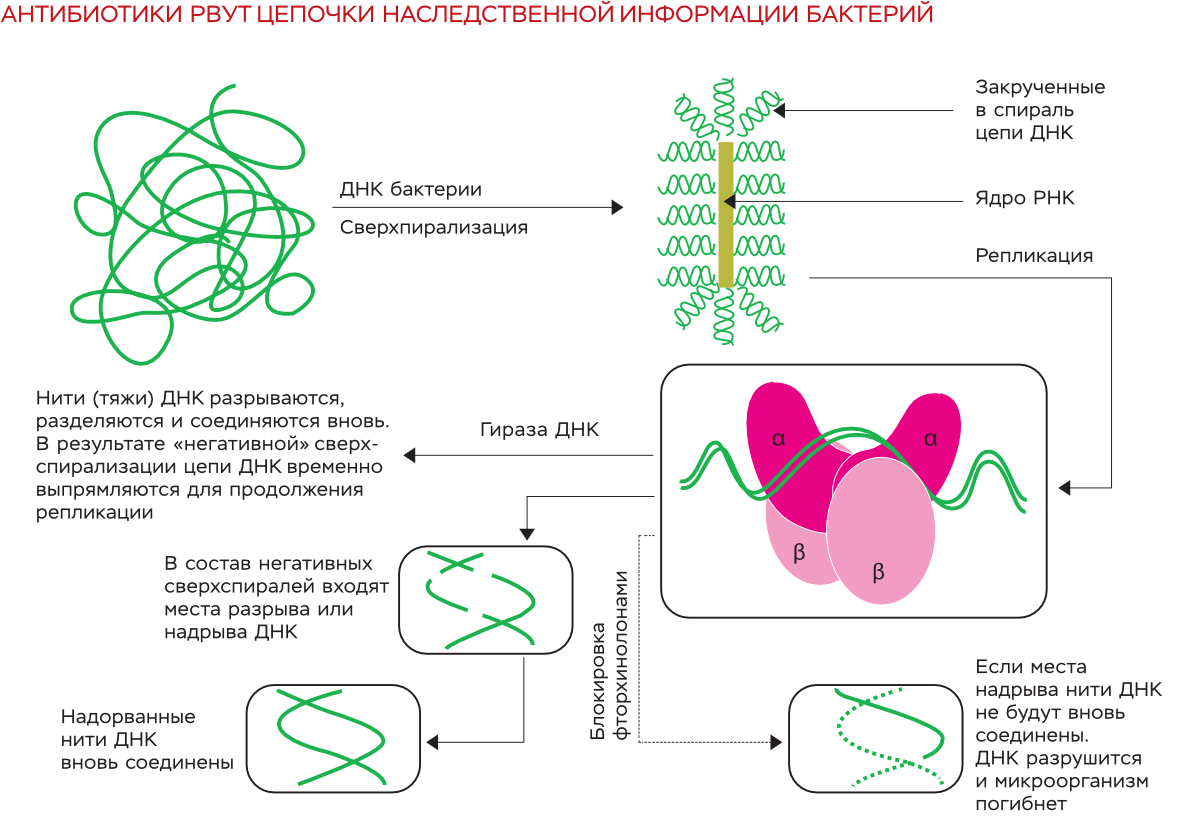
Как и у всех хинолонов и фторхинолонов, его действие направлено на ингибирование ДНК-гираз и бактериальной топоизомеразы IV, активность которых необходима для протекания таких фундаментальных процессов, как репликация и транскрипция. Из-за ингибирования этих ферментов невозможно свернуть обратно раскрученную суперспираль ДНК — «разрезать» ее гираза может, а вот «сшить» обратно — уже нет.
В ходе предыдущих исследований было выяснено, что большинство часто встречающихся побочных эффектов у пациентов, принимающих моксифлоксацин,— чувствительность к свету, тромбоз и прочее — вызвано неспецифическим взаимодействием препарата с клеточными оболочками. Теперь предстояло выяснить, что же именно происходит в клетке.
Клеточная мембрана человека включает в себя белки и жиры, которые в основном представлены фосфолипидами. Молекула такого липида состоит из полярной «головы» — фосфатной группы, которая обладает гидрофильными свойствами, и неполярных хвостов — длинных углеводородных цепей. Фосфолипиды образуют двойную структуру: гидрофильные остатки в сторону клетки и наружу, а между ними — прослойка из двух гидрофобных частей, называемая бислоем. В общепринятой у биологов жидкостно-мозаичной модели мембраны считается, что белковые молекулы растворены в жидком фосфолипидном бислое. Получающаяся тонкая мембранная пленка походит на мыльный пузырь — переливчатая, существующая в основном из-за сил поверхностного натяжения.
Чтобы изучить влияние антибиотика, в качестве модельной «клетки» организма-носителя исследователями использовалась липосома, сконструированная из дипальмитоилфосфатидилхолина (DPPC), окруженная стабильным частично проницаемым бислоем фосфолипида — кардиолипина (CL2-).
При pH = 7,4 — физиологическом значении кислотности в организме — моксифлоксацин существует в виде цвиттер-иона, то есть и карбоксильная группа, и аминогруппа заряжены. Последняя заряжена положительно, и из-за этого происходит образование комплекса моксифлоксацин — гидрофильный слой липидов. Этот вывод подтвержден методом ИК-спектроскопии, которая позволила уточнить, что связывание протекает между азотом моксифлоксацина с ацильными и фосфатными фрагментами кардиолипина, тогда как гидрофильная часть DPPC защищена положительно заряженной холиновой группой. К тому же, при исследовании образования комплекса фторхинолон—липидная оболочка в ультрафиолетовом диапазоне выяснено, что спектр излучения антибиотика становится менее интенсивным, что говорит об изменении его ионного состояния.
Механизмы воздействия антибиотиков
«Комплексообразование моксифлоксацина с липидным бислоем влияет на температуру фазового перехода клеточной мембраны: полное ожижение мембраны при добавлении антибиотика достигается при температуре на 2–3 градуса ниже, чем в контрольной системе, то есть нарушается ее текучесть,— рассказывает один из соавторов работы, сотрудник кафедры химической энзимологии химического факультета МГУ кандидат химических наук Ирина Ле-Дейген.— Из-за последующих нарушений подвижности белковых компонентов в жидком фосфолипидном бислое нарушаются важнейшие функции клеточных мембран — регуляторная, транспортная и защитная. Предположительно, в крайнем случае взаимодействие моксифлоксацина с отрицательно заряженной поверхностью мембраны может привести к разрушению целостности эукариотической клетки».
Как говорят авторы работы, данное исследование не просто позволяет лучше понять, как антибиотики, повсеместно применяемые для лечения теплокровных, могут негативно воздействовать на их организм. Речь идет об изменении направлений разработки новых антибиотиков на основе полученных данных. Скорее всего, изменения в формулах будущих препаратов будут направлены не столько на повышение их эффективности, сколько на уменьшение количества побочных эффектов. Меньшее количество сопутствующих воздействий может быть достигнуто и с помощью адресной доставки, которая на данный момент не применяется к хинолонам и фторхинолонам.

