Московские ученые совместно с зарубежными коллегами создали новый биосенсор для наблюдения за процессами метаболизма в живых организмах. Он обнаруживает сверхнизкие концентрации пероксида водорода, регулирующего обмен веществ. Изучать пероксид водорода трудно, ведь его молекулы живут максимум несколько секунд. Биохимический зонд HyPer7 оказался в 30 раз чувствительнее и в 80 раз быстрее предшественников. Исследования поддержаны грантом Российского научного фонда.
Перекись водорода — одна из важнейших молекул в организме живых существ. Она образуется в процессе метаболизма, а также выделяется специализированными ферментными системами. В организме это соединение регулирует работу различных биохимических процессов, но при слишком высоком его содержании может произойти так называемый окислительный стресс — избыток активных форм кислорода в организме. Он участвует в развитии многих заболеваний, таких как воспалительные, онкологические и нейродегенеративные. Регуляторную функцию молекулы выполняют, находясь в чрезвычайно низких концентрациях, из-за высокой скорости реакции они живут максимум несколько секунд. Эти особенности перекиси водорода сильно затрудняют изучение ее влияния на метаболизм и возникновение патологий.
Разработка российских ученых — плод многолетней работы над биосенсорами, позволяющими наблюдать за пероксидом водорода в клетке с помощью оптики, например микроскопа. Первое поколение отечественных зондов получило мировое признание и расширило знания ученых в области метаболизма, но имело существенный недостаток: они не могли обнаружить сверхнизкие концентрации H2О2, с помощью которых реализуется большинство ее функций. Также результаты наблюдения могли быть неточными из-за того, что работа сенсора сильно зависела от кислотности среды.
Обычно биосенсоры — это приборы, которые находят химические соединения с помощью веществ, реагирующих на эти соединения. Например, биосенсоры используются для измерения количества сахара или алкоголя в крови. Но биосенсоры, о которых идет речь в исследовании, являются белковыми молекулами. В основе такого зонда ученые использовали зеленый флуоресцентный белок GFP, способный поглощать свет и через несколько наносекунд испускать его обратно с немного увеличенной длиной волны, то есть «светиться». Такой белок сшивается с другим белком, OxyR, природным сенсором пероксида водорода. «Свечение» (флуоресценция) GFP меняет свойства при взаимодействии зонда с перекисью водорода. OxyR есть почти у всех бактерий. Поскольку исследователи не знали заранее, какой из белков окажется наиболее чувствительным, то выбрали для эксперимента 11 OxyR из разных неродственных друг другу видов микроорганизмов. В итоге сверхчувствительный сенсор получился при сшивании флуоресцентного белка GFP с белком OxyR, содержащимся в бактерии менингококк Neisseria meningitidis, обитающей в носоглотке человека и вызывающей менингит и назофарингит. OxyR этой бактерии реагирует на окисление пероксидом водорода, но при этом нечувствителен к другим активным формам кислорода.
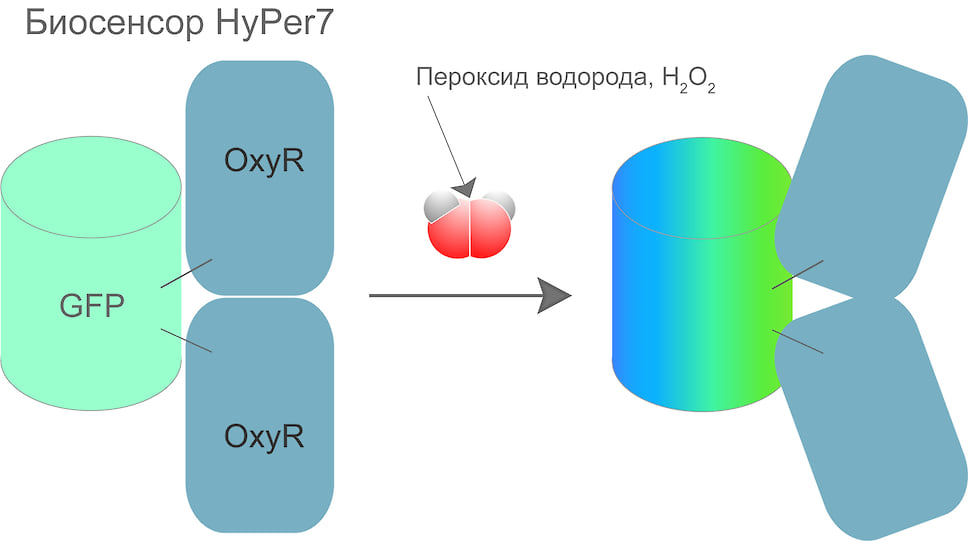
Биосенсор HyPer7 состоит из флуоресцентного белка GFP, сшитого с белком OxyR
Фото: Всеволод Белоусов
Биосенсор HyPer7 состоит из флуоресцентного белка GFP, сшитого с белком OxyR
Фото: Всеволод Белоусов
«По-видимому, менингококк в процессе эволюции выработал сверхчувствительный OxyR, строго избирательный к пероксиду водорода. Это нужно для того, чтобы заранее чувствовать активацию нейтрофилов и макрофагов, иммунных клеток организма хозяина, использующих пероксид водорода, чтобы убить бактерию. В ответ менингококк способен усиливать свои антиоксидантные системы, защищающие его от окислительного стресса»,— рассказывает Всеволод Белоусов, руководитель проекта по гранту РНФ, доктор биологических наук, заведующий отделом метаболизма и редокс-биологии ИБХ им. М. М. Шемякина и Ю. А. Овчинникова РАН, и. о. директора Федерального центра мозга и нейротехнологий Минздрава России.

Сотрудники отдела метаболизма и редокс-биологии ИБХ РАН в лаборатории. Слева – Валерий Пак, первый автор статьи
Фото: Из архива лаборатории
Сотрудники отдела метаболизма и редокс-биологии ИБХ РАН в лаборатории. Слева – Валерий Пак, первый автор статьи
Фото: Из архива лаборатории
По словам ученого, новый зонд HyPer7 — настоящий прорыв в сфере биосенсоров: «Мы получили уникальный индикатор с высокой яркостью и коротким временем отклика, реагирующий на сверхнизкие концентрации перекиси водорода, при этом не зависящий от кислотной среды. HyPer7 оказался в 30 раз чувствительнее и в 80 раз быстрее предыдущих версий».
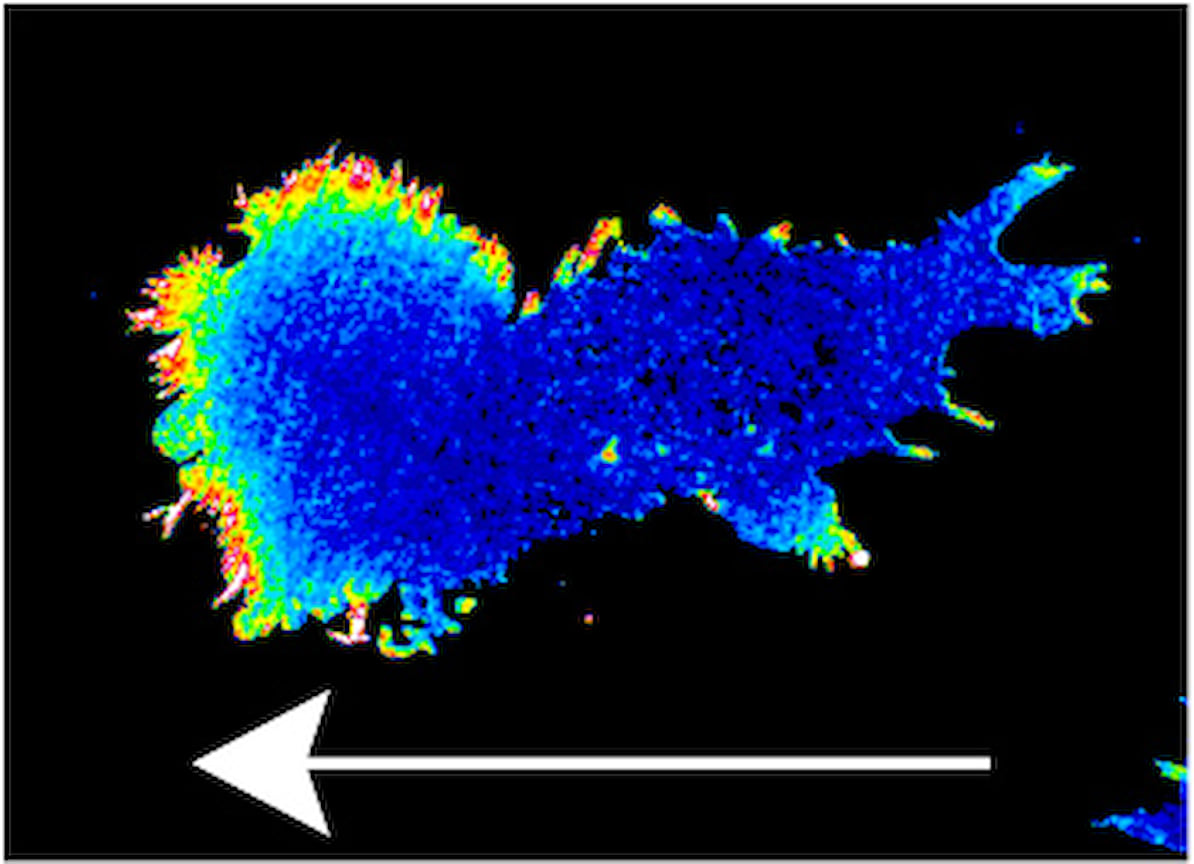
С помощью сенсора авторам работы уже удалось изучить детали перемещения молекул H2О2 внутри клетки, исследовать роль градиентов пероксида водорода в движении клеток и при повреждении тканей. Разработка биохимиков позволит визуализировать перекись водорода в клетках, тканях и органах и исследовать роль этой молекулы в нормальных биохимических процессах. Также будет изучена роль перекиси водорода в возникновении и развитии ишемических, нейродегенеративных, воспалительных и онкологических заболеваний, которые тесно связаны с окислительным стрессом. В исследовании российским ученым помогали коллеги из Бельгии, Франции, Германии и США.
По материалам статьи Ultrasensitive Genetically Encoded Indicator for Hydrogen Peroxide Identifies Roles for the Oxidant in Cell Migration and Mitochondrial Function; Valeriy V. Pak, Daria Ezeria, Olga G. Lyublinskaya, Sophie Vriz, Joris Messens, Vsevolod V. Belousov et al., журнал Cell Metabolism, март 2020 г.