«Наконец-то Нобеля по химии дали по химии!» — такими словами наполнились соцсети сразу после объявления лауреатов-2021 самой знаменитой научной премии. Оставим ученым споры про то, насколько неправа Шведская академия наук, которая с 1901 года примерно половину премий выдала за химические работы в области наук о живом. Тем более что все мы пользуемся результатами этих самых работ. Отметим лишь, что и открытия, сделанные лауреатами этого года, очень применимы в биологически активных молекулах.
6 октября 2021 года Шведская академия наук назвала имена лауреатов Нобелевской премии по химии. Ими стали профессор Кёльнского университета и директор Института исследования угля Общества Макса Планка (Германия) Беньямин Лист и профессор Принстонского университета (США) Дэвид Макмиллан. Как гласит формулировка, премия вручена «За развитие асимметричного органокатализа». Размер премии — 10 млн шведских крон.
«Катализаторы — одно из важнейших открытий, которое сделали химики,— говорит декан химического факультета МГУ, член-корреспондент РАН Степан Калмыков.— Дело в том, что нельзя просто смешать вещества А и В и ждать, что всегда получится нужное вещество С. Часто нужен определенный набор условий: температура, кислотность среды, правильное агрегатное состояние, давление, много времени. Критически важно порой отсутствие в реагентах примесей. Не менее важно вовремя удалять продукты реакции. Порой условия для проведения реакции нужны такие, что при них вещества вообще разлагаются. Еще чаще вместо нужной реакции начинает идти несколько других. Особенно часто такая ситуация встречается в органическом синтезе».
Классический пример — стрихнин, для первого синтеза которого в 1952 году потребовалось провести последовательно 29 (!) реакций. Выход от исходного вещества составил 0,0009%. Катализатор же обладает двумя замечательными свойствами. Он, во-первых, легко соединяется с одним из реагентов в комплекс, который так же легко реагирует со вторым реагентом. При этом катализатор (и это то самое «во-вторых») высвобождается в первоначальном виде. В результате несколько обходных стадий реакции заменяются на одну прямую. В случае стрихнина 29 реакций схлопнулись до 12 (!), а количество полученного вещества увеличилось в 7 тыс. раз.
То, что одни вещества могут реагировать с другими, химики знали давно. Неожиданностью стал ряд наблюдений, сделанных в начале XIX века: оказалось, что одни вещества начинают быстрее реагировать в присутствии других веществ. Но не с ними. Например, перекись водорода начинала быстрее разлагаться в серебряной посуде, при этом серебро не растворялось. В 1835 году известный шведский химик Яков Берцелиус впервые показал некоторые закономерности этого процесса, указал на его обширность и, собственно, ввел понятие «катализатор».
Ученые всего мира бросились на поиски катализаторов. В результате им удалось выделить две большие группы катализаторов — металлы и ферменты. Перечислять все Нобелевские премии по химии, которые связаны с обеими группами катализаторов, слишком долго, но несколько из них все же стоит назвать. Например, Эдуард Бюхнер научился перерабатывать сахар в спирт без дрожжей. А затем за изучение выделенных им ферментов еще двое получили Нобелевку. Благодаря открытому Полем Сабатье механизму реакции стали делать маргарин. А Вильгельм Освальд, например, придумал, как легко при помощи катализаторов соединить водород и азот, и теперь так делают 180 млн тонн аммиака в год.
Сказать, что катализаторы активно используются в нашей жизни, мало. Треть промышленной химии делается при помощи катализаторов. Переработка тяжелых фракций нефти тоже катализаторы. В каждом автомобиле с двигателем внутреннего сгорания стоит дожигатель выхлопных газов. Большинство лекарств делается с помощью катализаторов.
Правда, с биологически активными веществами все оказалось несколько сложнее. Оказалось, что в нашем организме важен не только набор функциональных групп, но и их взаимное расположение. Причем критически важным оказалось то, как они присоединены к одному и тому же атому углерода.
Посмотрите на свои руки. Такие одинаковые и такие разные. То, что вы видите, называется примером «зеркальной» симметрии. Правая рука может совпасть только с отражением левой руки в зеркале, но не с самой левой рукой. В органической химии тоже есть такие «правые» и «левые» руки. У них атомный (элементный) одинаковый состав, одинаковый набор функциональных групп, и расположены они на одних и тех же атомах углерода. Но только в зеркальном отражении. Из-за такой пространственной изомерии они проявляют себя в живом организме по-разному. Например, L-карнитин помогает нам расщеплять жиры. Его оптический изомер D-карнитин — яд. Есть и другие пары, в которых один изомер — лекарство, а второй откровенно токсичен. Самый известный из них — талидомид, седативный препарат, который с успехом применяли беременные женщины в 1957–1962 годах. Оказалось, в организме он изомеризовался, а его изомер нарушал развитие плода и вызывал физические уродства. Это, кстати, одна из причин, почему сейчас все медицинские препараты тестируются так долго.
Для синтеза биологически активных веществ правильного строения металлические катализаторы не подходят. Они или слишком чувствительны к воде, кислотности, кислороду и т. д., или очень дорогие: платина, палладий, рений. И довольно токсичны. Ферменты тоже довольно дорогие и к тому же очень сложные молекулы. Правда, не весь фермент реагирует с другими молекулами, а только его активный центр. И тут у Беньямина Листа зародилась идея: что если синтезировать этот самый активный центр отдельно? Возможно, все это нагромождение аминокислот с кучей атомов металла и не нужно для того, чтобы катализировать нужный процесс? Он попробовал провести эксперименты с простой молекулой — пролином. И получил потрясающий результат. Катализатор сработал.
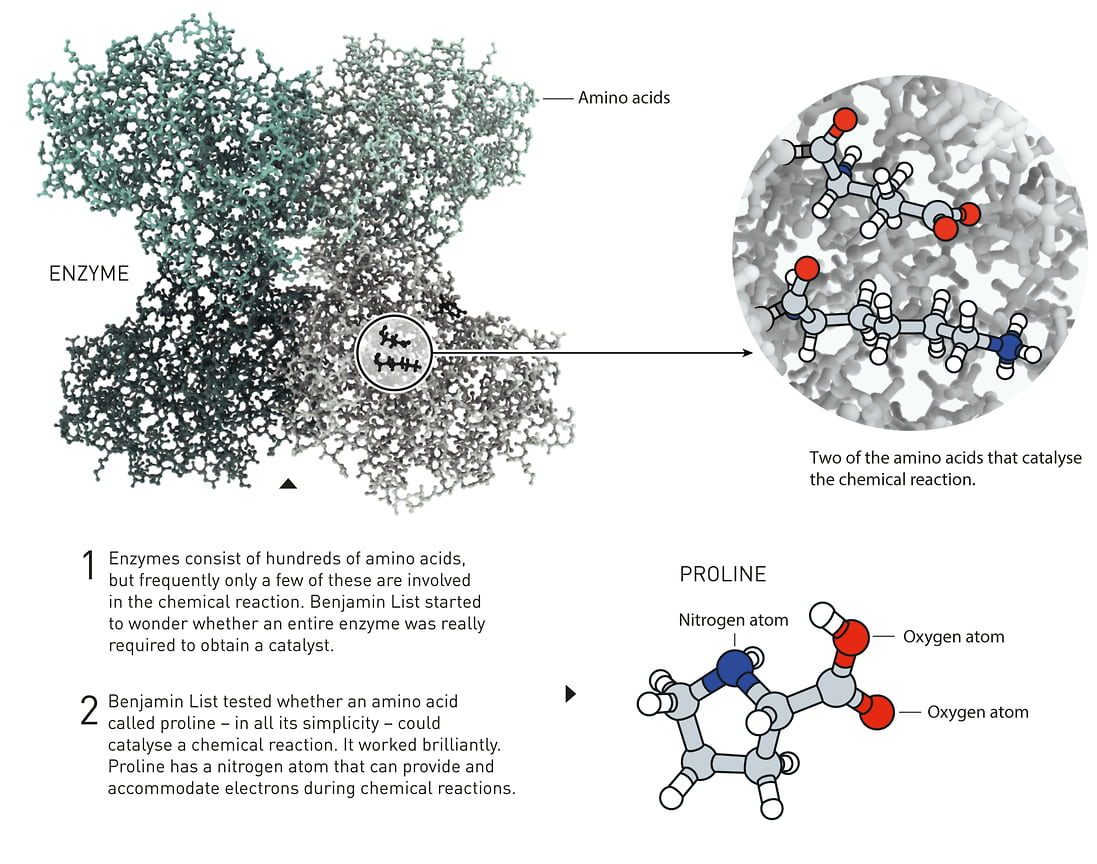
Фото: The Royal Swedish Academy of Science
Фото: The Royal Swedish Academy of Science
В это самое время в Беркли Дэвид Макмиллан подошел к вопросу с другой стороны. Работая над металлическими катализаторами, он подумал: а так ли нужен для катализа этот ядовитый и дорогой атом металла? Может, можно использовать атом неметалла, способный отдавать и принимать электроны? Взяв за основу азот, он получил так называемый иминий-ион, который также справился с задачей. Катализатор собрал из двух органических молекул структуру с шестичленным кольцом (реакция Дильса-Альдера), но быстрее и легче.
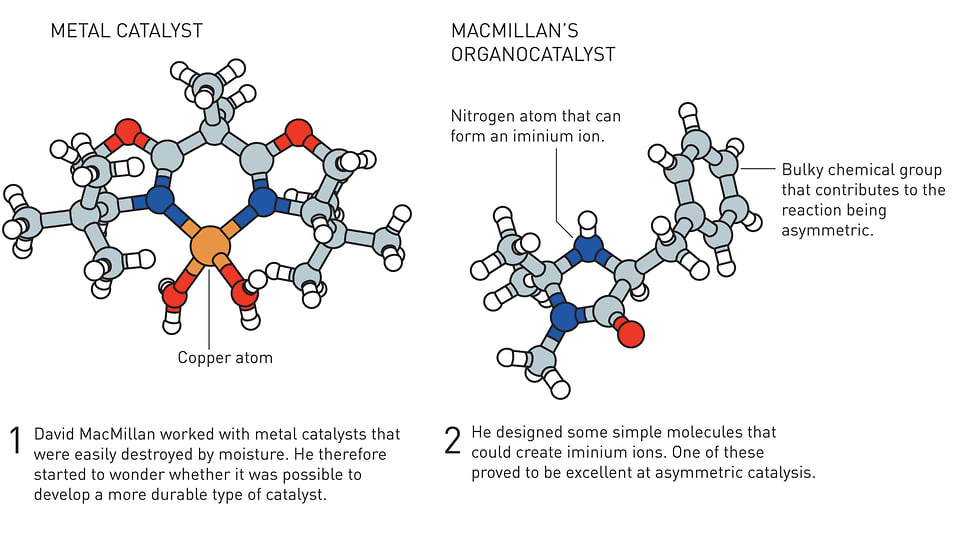
Фото: The Royal Swedish Academy of Science
Фото: The Royal Swedish Academy of Science
Оба исследователя показали, что безметаллические органические катализаторы из простых молекул способны направлять синтез биологически активных молекул строго определенной конфигурации. «Эта концепция катализа настолько же проста, насколько и гениальна, и факт в том, что многие люди задавались вопросом, почему не подумали об этом раньше»,— сказал председатель Нобелевского комитета по химии Йохан Аквист.
Открытие спровоцировало настоящую «золотую лихорадку». И сейчас огромное количество сложных лекарств на основе человеческих ферментов производится при помощи этих катализаторов. Да и вообще меняются промышленные процессы на заводах по производству множества органических соединений. А весь с точки зрения науки в этой области еще многое не изучено. Так что потенциал есть и для ученых, и для промышленности.

