Группа ученых из Центрального НИИ стоматологии и челюстно-лицевой хирургии разработала материал, способный эффективно восполнять костную ткань в области обширных дефектов. Работа поддержана Российским научным фондом.
Ранее для решения подобных задач врачам приходилось использовать костную ткань, забранную непосредственно от пациента из ребра, берцовой и подвздошной кости. В случае восполнения дефектов небольшого и среднего размера удавалось обходиться костной тканью, полученной из других участков челюсти. Но даже в этом случае пациент был обречен на дополнительную травму, вызванную формированием обширного донорского участка. Все это осложняло период восстановления пациента и сопровождалось отеком, кровопотерей и риском инфицирования зоны забора трансплантата.
Почему еще не существует материалов, способных удовлетворительно заменить костную ткань? На самом деле они существуют, но все неидеальны. Самый распространенный — швейцарский Bio-Oss. Его могут предложить практически в любой клинике, которая занимается установкой зубных имплантатов. Это минеральный компонент, полученный из кости быков. Его достоинство — отсутствие органического компонента, который мог бы вызвать иммунный ответ и отторжение материала, а также подражание структуре костного матрикса человека.
Однако этот материал лишь наполнитель, сам по себе он не способствует образованию костной ткани. До недавнего времени подобное было по плечу только собственной костной ткани человека. Причина в том, что наши кости содержат специальные белки, которые называют остеоиндукторами. При повреждении кости, например при переломе, они выходят из нее и сигнализируют стволовым клеткам, что сюда нужно прийти, превратиться в специализированные клетки и образовать костную ткань. Поэтому даже при использовании костного материала Bio-Oss врач вынужден добавлять в него собственную костную ткань пациента, иначе нормальная кость не будет образована, а дефект заместится рубцом. Все это требует от врача, пусть уже в меньшей мере, прибегать к дополнительной травме для забора собственной костной ткани пациента.
В США недавно было налажено производство материала InfuseBoneGraft, который содержит тот самый, необходимый для стимулирования регенерации кости остеоиндуктор. Материал представляет собой губку, пропитанную высококонцентрированным раствором остеоиндуктора BMP-2 (костный морфогенетический белок-2), самым мощным из ныне изученных.
В России препарат еще не лицензирован. И вряд ли будет. Дело в том, что первый блин получился комом. Контейнер для доставки активного компонента был выбран не очень удачно, и при внесении в рану происходит вытекание из него раствора, который может случайно попасть за пределы костного дефекта и спровоцировать там нежелательное формирование кости. Кроме того, материал содержит избыточное количество BMP-2, и в области его применения может произойти формирование излишнего объема костной ткани, что может привести к деформации челюсти, смещению установленных имплантатов или даже спровоцировать рост опухоли.
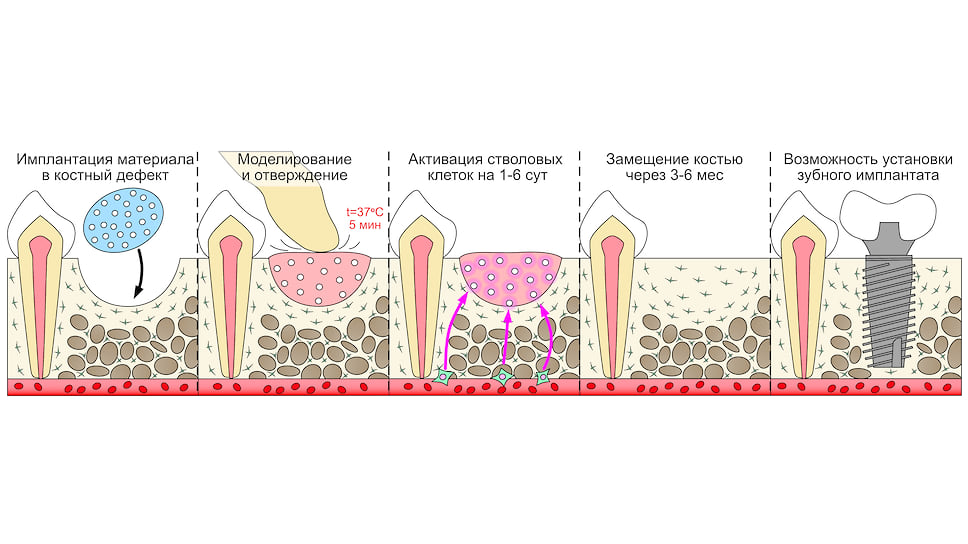
Российские ученые разработали более сложный материал, который состоит из трех компонентов. Первый — это моделируемая матрица. Она позволяет материалу отверждаться после внесения в рану и сохранять заданную форму на всем протяжении срока восстановления. За счет этого врач может отказаться от дополнительных армирующих конструкций, в качестве которых обычно используют титановые сетки и металлические винты. Их извлечение после формирования костной ткани травматично для пациента и неудобно врачу. Второй компонент — упрочняющий наполнитель, который добавляет материалу эластичности и прочности, а также позволяет выдерживать высокие нагрузки, которым противостоит костная ткань. И третий, самый важный компонент — контейнер для доставки остеоиндуктора, который способствует его выходу в нужный момент процесса регенерации. Дело в том, что первые сутки после травмы, вызванной операцией имплантации костного материала, организм занят защитой области вмешательства, что проявляется в виде небольшого воспаления. И только спустя несколько суток процесс воспаления завершается и наступает период построения новых тканей и регенерации. Именно в этот момент действие остеоиндуктора является наиболее эффективным, а значит, для активации роста новой кости его требуется меньше.
Для работы в проекте были привлечены специалисты из Курчатовского института и ФГБНУ "Медико-генетический научный центр им. академика Н.П. Бочкова". Руководят проектом академик РАН Анатолий Кулаков и профессор Дмитрий Гольдштейн. Анатолий Кулаков — один из пионеров в области зубной имплантологии, а Дмитрий Гольштейн — специалист в области регенеративной медицины. Оба руководителя хорошо известны в России и за рубежом как видные ученые. Образование коллабораций между представителями различных сфер науки позволило решить трудные и прежде непреодолимые для отдельных научных коллективов задачи. В проект были вовлечены молодые ученые: к.м.н. А. В. Васильев, к.б.н. Т. Б. Бухарова, к.ф-м.н. Т. Е. Григорьев и аспиранты Ю. Д. Загоскин и В. С. Кузнецова.
Полную структуру материала исследователи пока не раскрывают. Однако известно, что основные компоненты материала — термоотверждаемый хитозановый гель, высокопористые полилактидные гранулы и сильнейший остеоиндуктор BMP-2. Главным достижением проекта можно считать то, что ученым удалось совместить эти компоненты таким образом, что они улучшили свойства друг друга. Хитозановый гель требовал особой модификации для улучшения его биологических свойств. Полилактидные гранулы способствовали длительному высвобождению остеоиндуктора, с одной стороны, а с другой — взаимодействуя с гелем хитозана, повышали его прочность, пластичность и биосовместимость.
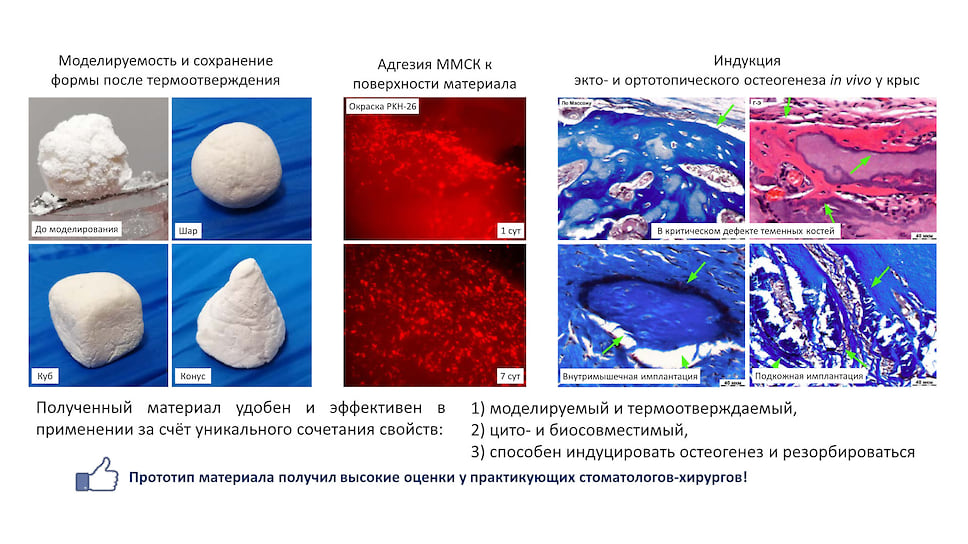
Разработанный материал в ходе физико-механических испытаний показал способность отверждаться при температуре 37 градусов уже через пять минут после окончания моделирования его формы. То есть после внесения в рану материалу можно задать сложную форму костных дефектов, которую материал будет сохранять на протяжении всего периода замещения костной тканью.
При исследовании на лабораторных животных материал активировал рост костной ткани даже при подкожном и внутримышечном введении, то есть заставлял кость расти в тех условиях, где организм ее не сформировал изначально. При внутрикостном введении в области дефектов черепа и челюстей лабораторных крыс и карликовых свиней материал также способствовал активному росту кости. Проектируемый материал также показал свою эффективность в процессе исследования на выделенных из человека культурах клеток.
Впереди проведение регистрационных испытаний и внедрение остеопластического материала в медицинскую практику.