Обычно молчаливо предполагается, что главные проблемы современной физики лежат в области микромира (физика элементарных частиц, стандартная теория взаимодействий и т.д.), либо в области "мега-мира" (проблемы темной материи, черные дыры, модели Вселенной). Но в окружающем нас обычном макромире существуют объекты, которые до сих пор не имеют адекватного описания на микроскопическом уровне. Это обычные жидкости. Жидкость — классическое агрегатное состояние вещества — в отличие от твердых тел и газов до сих пор является источником головной боли для экспериментаторов и особенно для теоретиков. Как ни странно, с математической точки зрения причины сложности описания жидкости схожи с теми, что имеются в физике элементарных частиц или в космологии, — а именно, сильные нелинейности и отсутствие малого параметра. Для жидкостей это означает близкие значения кинетической и потенциальной энергий атомов или молекул. В кристалле преобладает потенциальная энергия взаимодействия между атомами, в газе — кинетическая.
Парадокс жидкостей заключается еще и в том, что при нормальных земных условиях они не должны существовать. Вещества с сильными межатомными взаимодействиями (ковалентное, ионное, металлическое) должны быть твердыми, со слабыми (ван-дер-ваальсовое, молекулярное) — газами. Не случайно среди более чем сотни элементарных веществ в жидком состоянии при нормальных условиях находятся всего два — ртуть и бром. Обратная сторона этого парадокса состоит в том, что повсюду, в том числе в быту, нас окружает огромное количество жидкостей (уже не элементарных). Из них исключительную роль играет вода.
Жидкость теоретиков и жидкость экспериментаторов
Теоретическое описание жидкостей стартует, как правило, с газового состояния, а потом плавно "включается" взаимодействие частиц. В пользу такого "газового" подхода говорят текучесть жидкостей, их малая вязкость, отсутствие сдвиговой жесткости, кажущаяся бесструктурность жидкости, непрерывный переход в закритической области. "Маленький" минус такого описания состоит в том, что энергия взаимодействия частиц, рассматриваемая как слабое возмущение на фоне "главной" кинетической энергии, на самом деле в несколько раз ее превышает.
В то же время, с точки зрения экспериментаторов, жидкость вблизи температуры плавления имеет много черт, роднящих ее с твердым телом. Это прежде всего малые скачки большинства характеристик при плавлении, несмотря на потерю дальнего порядка. Жидкость имеет почти твердотельные значения плотности, теплоемкости и многих других свойств. Непрерывный переход в твердое стекло при охлаждении многих жидкостей также свидетельствует о родстве жидкого и твердого состояний.
Прогресс в теоретическом описании жидкостей за последние 100 лет оказался весьма скромным. Исходя из потенциала взаимодействия атомов (молекул) жидкости, можно описать плотный газ и окрестность критической точки. Теория может также предсказать структуру простых жидкостей типа аргона (она похожа на хаотическую плотную упаковку шаров), однако структуру более сложных жидкостей — расплавов металлов, молекулярных и ковалентных жидкостей — описать не удается. Еще хуже обстоит дело с описанием микроскопической динамики (то есть движения частиц в жидкостях) и коротковолновых возбуждений, а также с количественными предсказаниями теплоемкости и многих других свойств.
Получается, что параллельно существовало как бы два разных класса жидкостей — "жидкости для теоретиков", похожие на плотный газ, и "жидкости для экспериментаторов", похожие на твердое тело.
Ни сильная, ни слабая
Жидкий беспорядок и жидкий порядок
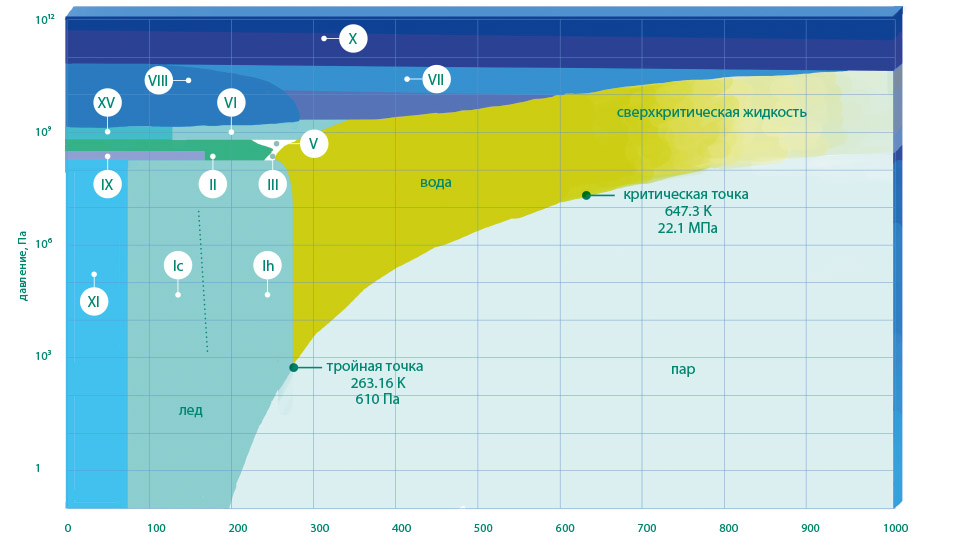
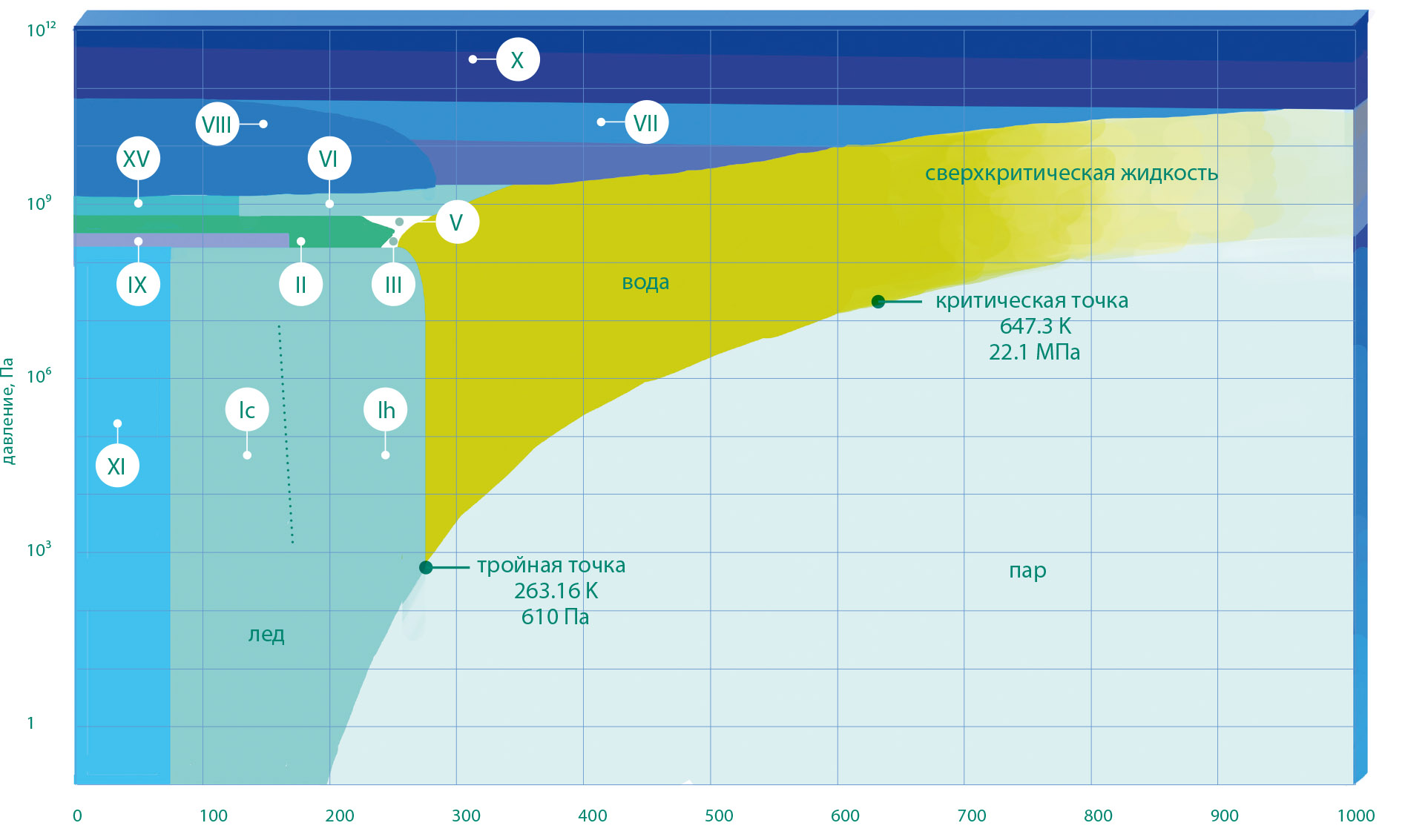
В последние десятилетия физики подвергли сомнению такую основную газоподобную черту жидкости, как ее бесструктурность. Было установлено, что в жидкостях наблюдается некий "мотив" в местонахождении соседних частиц — так называемая структура ближнего и промежуточного порядка. Рассмотрим, например, расплавленное железо и молекулярный жидкий азот. Это жидкости с совершенно разными свойствами и структурами, при изменении давления и температуры их поведение, конечно, тоже должно отличаться. Во многих кристаллах при изменении физических условий происходят фазовые переходы. Известно, например, что графит под давлением превращается в алмаз. И это скорее правило, чем исключение: почти все кристаллы при сжатии неоднократно кардинально меняют структуру и свойства. Например, обычный водяной лед при высоких давлениях может превращаться в 14 (!) различных модификаций. Оказалось, что при сверхвысоких давлениях во многих жидкостях также наблюдаются фазовые превращения, которые сопровождаются изменениями их структуры и свойств. Например, в расплаве сульфида мышьяка при сжатии может происходить несколько последовательных превращений с изменением структуры ближнего порядка: тип связи последовательно изменяется от молекулярного к ковалентному, затем к металлическому. При фазовых превращениях в жидкостях под давлением их электропроводность и вязкость может меняться в тысячи раз.
Эти данные важны не только для физики, но и для геологии и планетологии, так как многие соединения в недрах Земли и других небесных тел находятся в жидком состоянии. Отрадно, что в области изучения фазовых переходов в жидкостях российские физики фактически определяют мировой уровень.

Семьдесят аномалий
Линия раздела в сверхкритическом флюиде
В последние годы был также развеян миф об отсутствии в жидкостях сдвиговой жесткости. Из школьной физики известно, что поперечные волны в жидкостях, как и в газах, не распространяются. В то же время физикам давно известно, что высокочастотные ультразвуковые поперечные волны прекрасно распространяются через вязкие жидкости, такие как мед. Благодаря работам итальянских и французских физиков в последние два десятилетия было установлено, что на терагерцовых частотах сдвиговую жесткость имеют все жидкости, независимо от их вязкости.
Большое число примеров изменения структуры и свойств жидкостей при очень высоких давлениях и температурах заставляет задуматься о поведении жидкостей в сверхкритическом состоянии. Со школы всем известно, что кривая перехода жидкость — газ (кипение) заканчивается в критической точке и при давлениях и температурах выше этой точки они неразличимы между собой. Такое состояние вещества принято называть сверхкритическим флюидом. В последние годы исследования таких флюидов вышли на новый уровень из-за их широкого промышленного использования. Вещества в этих особых состояниях имеют свойства чрезвычайно активных растворителей. Они применяются для переработки отходов, экстракции (в химической и фармакологической индустрии), в качестве реакционных сред.
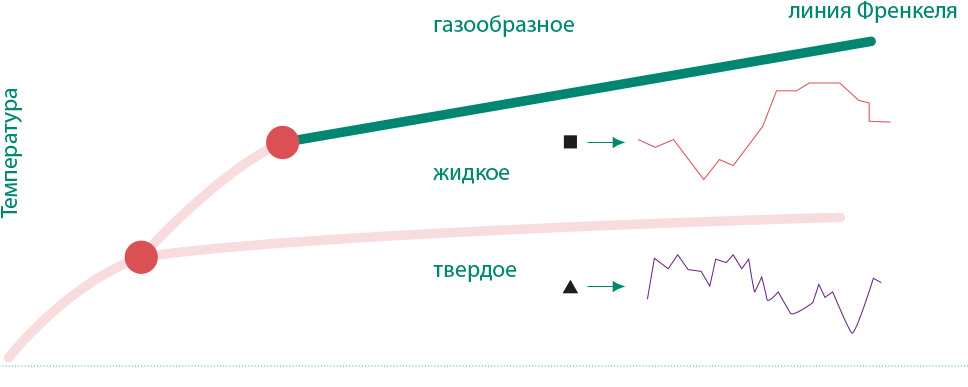
Многие из изученных фазовых превращений в жидкостях происходят при давлениях и температурах намного выше критических, где, казалось бы, все жидкости должны терять "индивидуальность", однако этого не происходит. В последние годы наша группа активно изучала жидкое состояние при температурах, в сотни раз превышающих критические, и давлениях, в десятки тысяч раз больше критических. Так как экспериментальные возможности изучения жидкостей при таких экстремальных параметрах сильно ограничены, одним из основных методов исследований стало компьютерное моделирование свойств жидкостей с использованием суперкомпьютеров. Как это ни удивительно, оказалось, что качественные различия между жидкостью и газом в сверхкритической области сохраняются. Наиболее важное различие состоит в характере траекторий частиц. Движение атомов в жидкости представляет собой почти гармонические колебания с малой амплитудой — и относительно редкие прыжки на большие расстояния. В газе частицы между столкновениями перемещаются почти свободно. В ходе исследований мы установили, что так называемая линия смены типа траекторий частиц существует и в закритической области, при сколь угодно больших давлениях и температурах. Я предложил назвать ее "линией Френкеля", в память о заслугах выдающегося советского физика. Смена типа динамики частиц приводит к ряду важных следствий. Во-первых, флюид теряет сдвиговую жесткость на всех возможных частотах. Таким образом, разные агрегатные состояния можно отличить друг от друга, используя достаточно строгий критерий: твердое тело имеет сопротивление сдвиговой деформации на всех доступных частотах, жидкость — только на высоких, а газ — ни на каких! Во-вторых, в окрестности линии Френкеля качественно меняются температурные зависимости всех основных свойств флюида — вязкости, скорости звука, теплопроводности и т.д. В-третьих, теплоемкость в расчете на частицу на линии Френкеля является практически универсальной величиной и близка к удвоенной константе Больцмана (в расчете на частицу для моноатомных флюидов).
Исследования при сверхвысоких давлениях раскрывают нам причины сложности теоретического описания жидкостей. Твердые тела и газы в каком-то смысле можно назвать "чистыми" агрегатными состояниями. В кристаллах, стеклах динамика движения частиц колебательная, в газах — столкновительная. Жидкость представляет собой "смешанное" агрегатное состояние — переходное от твердого к газообразному. В ней присутствуют оба типа движения — колебательное и баллистическое, и их взаимная доля плавно меняется при изменении внешних параметров. В этом феномене одна из главных причин, почему микроскопическая динамика жидкого состояния трудно поддается теоретическому описанию. То есть теоретики и экспериментаторы фактически имели дело с "разными жидкостями". Теоретики хорошо описывали плотный газ выше линии Френкеля, где теплоемкость меняется от 1,5 до 2 констант Больцмана, четкий ближний порядок отсутствует, поперечные возбуждения не распространяются. Экспериментаторы же, как правило, исследуют жидкости ниже линии Френкеля с теплоемкостью от 3 до 2 констант Больцмана на частицу, сдвиговой жесткостью на высоких частотах, определенной структурой ближнего порядка и т.д. Таким образом, различие между жидкостью и газом существует при любых внешних параметрах, просто выше критической точки переход из одного состояния в другое происходит без термодинамических аномалий. Можно быть уверенным, что дальнейшие экспериментальные и теоретические исследования флюидов при сверхвысоких давлениях принесут еще немало сюрпризов. Жидкости только начали делиться с нами своими секретами.
Рис. 04 Предполагаемое положение линии Френкеля