Ученые, чьи исследования послужили основой для разработок компании "Гурус биофарм", работают вместе с середины 1980-х годов: Владимир Безуглов в Институте биоорганической химии им. академиков М. М. Шемякина и Ю.?А. Овчинникова РАН, а его бывший аспирант Игорь Серков — в ИФАВ РАН; то есть уже тридцать лет они занимаются синтезом модифицированных простагландинов.
На первом этапе работы группе Безуглова удалось фторировать простагландины — заменить на фтор гидроксильные группы. После такой модификации простагландины стали действовать избирательно и оказались более устойчивы к действию метаболических ферментов. Но не только: научившись заменять фтором любую из гидроксильных групп, ученые выяснили, какую роль эти группы играют в механизме действия природных простагландинов.
Вроде бы можно было начинать доклинические испытания тех или иных вариантов фторированных простагландинов — но этого сделано не было. Медики опасались, что ядовитый и химически очень активный фтор, включившись в метаболизм, может образовать в организме новые соединения с совершенно непредсказуемыми свойствами.
А рисковать ученым не хотелось. Тогда они задались вопросом, чем можно заменить гидроксильные группы, чтобы, с одной стороны, повысить эффективность и избирательность действия простагландинов; а с другой — воспользоваться их универсальностью и одним препаратом воздействовать на несколько целей в организме.
Сейчас в фармацевтике доминирует концепция "одна болезнь — одна мишень — одно лекарство". Генная инженерия, технологически очень продвинувшаяся в последнее десятилетие, сделала эту концепцию чуть ли не единственно возможной. В самом деле, уже вполне можно рассчитывать, что действующее вещество попадет в конкретное место молекулы конкретного белка и окажет там уникальный лечебный эффект, не вызвав никаких побочных явлений; ясно же, какой сверхвысокой селективности достигает в таком случае фармацевтический препарат!
Но тяжелые хронические заболевания — вроде атеросклероза, нейродегенеративных, онкологических или аутоиммунных патологий — затрагивают множество органов и тканей, для лечения приходится использовать такое же множество фармацевтических препаратов. Но комбинация из нескольких высокоселективных лекарств, к сожалению, может быть убийственно опасной.
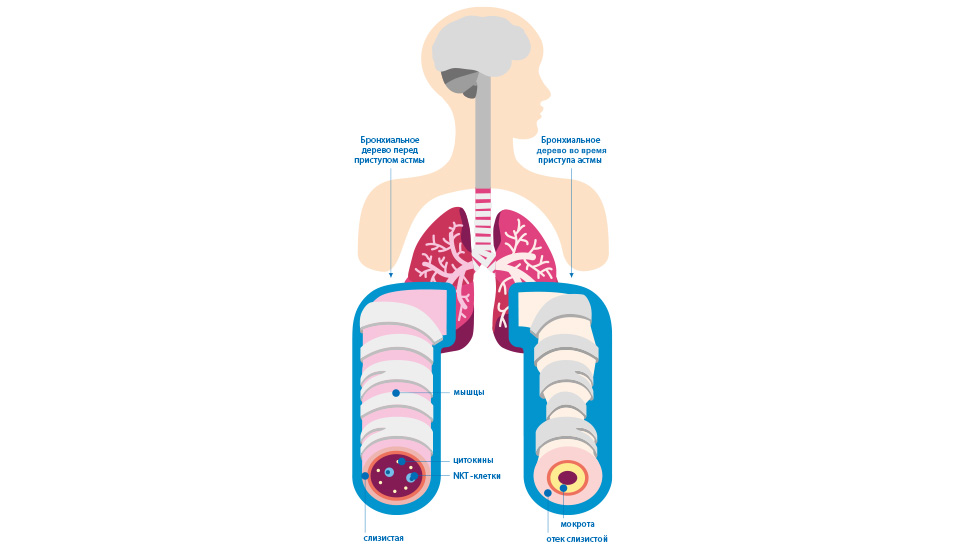
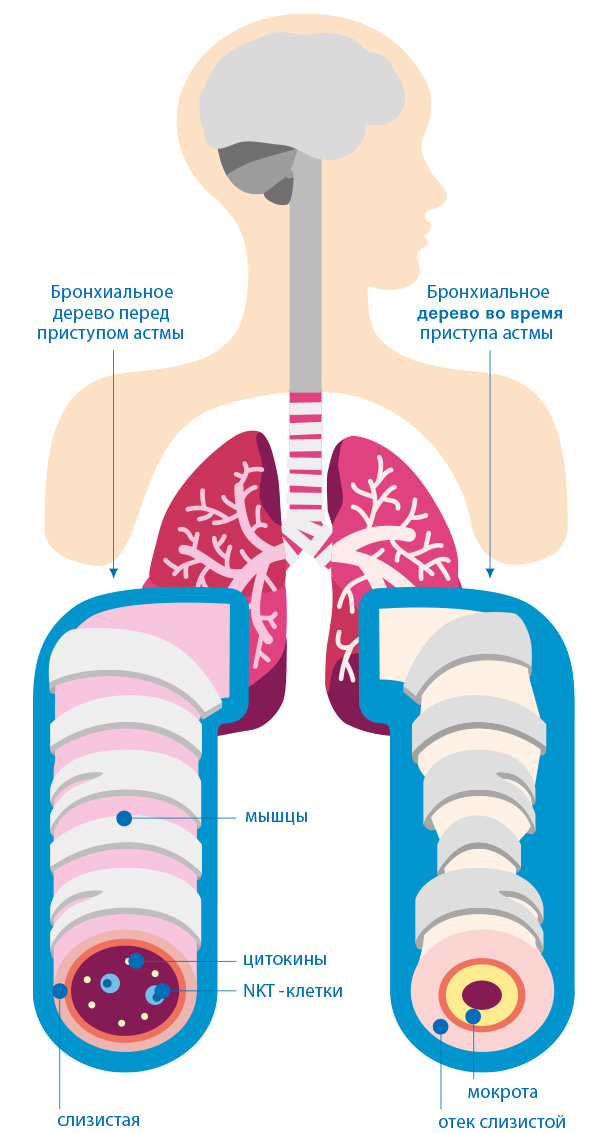
Группа Безуглова разрабатывает полифункциональные препараты: раз многие сложные заболевания, к примеру астма [рис. 01 — стр. 19], носят системный характер, то и действовать надо системно, вовлекать в лечебный процесс максимум органов и тканей, пораженных болезнью, — но за счет одного препарата, а не горсти таблеток три раза в день после еды.

Дыши, мышь
Создатели "Гурус биофарма" приводят простую аналогию: поддержать потерявшего равновесие человека ладонью куда проще, чем пальцем. "Болезнь напоминает корабль, получивший несколько пробоин, а применение монофункциональных препаратов напоминает заделывание одной из пробоин, хотя из других течь продолжается, — приводит другую аналогию гендиректор компании, кандидат биологических наук Игорь Любимов. — Команда будет постоянно вычерпывать воду, затекающую из оставшихся пробоин, но корабль утонет, когда команда устанет. Вычерпывание воды — это симптоматическая терапия. Когда заделаны все основные пробоины, корабль сохранит живучесть надолго. Это и делают мультифункциональные лекарства".
Простой способ получить полифункциональный препарат — смешать несколько монофункциональных; но сочетание может быть опасным. Сложней соединить несколько фармакофоров, то есть действующих веществ, в одной молекуле: собрать несколько молекулярных фрагментов, каждый под свою мишень, но так получаются препараты с множеством непредсказуемых побочных эффектов. Нужно идти дальше — сконструировать молекулу, где компоненты будут эндогенными веществами.
"Гурус биофарм" как раз и создал подобную гибридную молекулу: в природный простагландин E2 введены оксид азота и глицерин. Этот простагландин E2 вообще-то отлично расширяет бронхи, но его ингаляция вызывает сильный кашель, а это чрезвычайно опасно для пациентов с астматическим приступом. Но в комбинации с оксидом азота и глицерином воздействие на кашлевые рецепторы устраняется, а бронхорасширяющий эффект остается. Простую молекулу оксида азорта "привязать" к простагландину нельзя, поэтому в "Гурус биофарме" использован "донор" — вещество с двумя NO на молекулу. Глицерин же несложно связать с липидом. Препарат получил название "нитропростон".

По пути французов
Гибридная молекула действует сильнее отдельных компонентов. Например, мы вводим в тест-систему сам простагландин и определяем, что для расслабления трахеи нужна доза 20 условных единиц (у. е.) концентрации. Когда мы вводим одновременно, но отдельно простагландин и доноры NO, доза падает до 10 у. е., а если нитропростон, эффективная доза снижается до 1 у. е., объясняют создатели. Дело в том, что молекула простагландина адресно доставляет молекулу NO (это очень короткоживущее соединение — распадается в организме за 6-10 секунд) и запускает процесс ее отщепления именно в гладких мышцах бронхов.
На данный момент эта разработка для лечения бронхиальной астмы запатентована и в России, и за границей. Впереди — 6-12 лет для вывода лекарственного препарата на рынок; в скором времени начнутся доклинические исследования нитропростона уже в комбинациях с препаратами, применяемыми сегодня для лечения бронхиальной астмы.
Владимир Безуглов и Игорь Серков первоначально работали над темой химической модификации биоэффекторных липидов на государственные деньги и с привлечением грантов, сейчас исследования продолжаются уже на средства "Гурус биофарма" — инвестиции компании составили подавляющую часть из общей суммы 18 млн руб.
Рис. 01 Бронхиальная астма
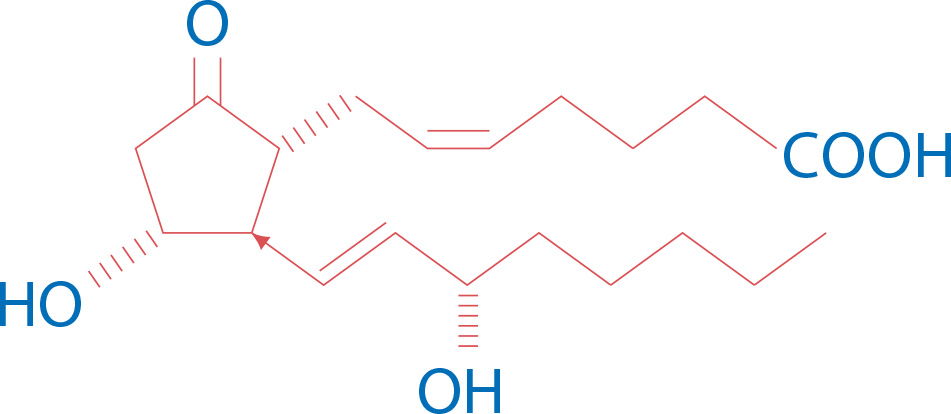
Таб. 01 Химическая формула простагландина E2
Что такое простагландины
Простагландины — группа липидных физиологически активных веществ. Синтезируются во многих органах и тканях из полиненасыщенных жирных кислот при необходимости, распадаются чрезвычайно быстро, поэтому действуют — в отличие от гормонов — только вблизи места секреции, активны в низких концентрациях (10-9М и менее). Открыты шведским физиологом Ульфом фон Эйлером в семенной жидкости, поэтому название происходит от предстательной железы (glandula prostata). Простагландины участвуют в поддержании гомеостаза организма (например, участвуют в механизмах сужения и расширения сосудов); в воздействии на болевые рецепторы; в регулировании иммунного ответа; в оплодотворении яйцеклетки, поддержании жизнедеятельности плода и родовой деятельности; вызывают сокращение или расширение (простагландин Е2) бронхов и трахеи; усиливают воспалительную реакцию, вызванную ожогами и повреждениями (аспирин ослабляет воспалительное состояние, потому что необратимо ингибирует циклоксигеназу, без которой синтез простагландинов невозможен); обусловливают повышение температуры тела; оказывают седативное и транквилизирующее действие; стимулируют секрецию ферментов поджелудочной железы; тормозят желудочную секрецию; обладают противовирусной и противоопухолевой активностью.



